
FUNDAMENTO TEÓRICO
Los densímetros son aparatos que miden la densidad de los líquidos fundándose en el Principio de Arquímedes. Están formados por varillas de vidrio hueco que presentan un ensanchamiento en la parte inferior y un lastre. Al sumergirlas en un líquido flotan, cumpliéndose que el peso del volumen de líquido desalojado es igual al peso de todo el aparato; por tanto, se hundirán más o menos según sea la densidad del líquido.
Los densímetros vienen graduados directamente en densidades (g/cm3). Existen dos tipos de densímetros:
a) Para líquidos más densos que el agua (fig. 21.1) que llevan la indicación 1 en la parte superior de la varilla. Esta señal corresponde a la parte sumergida cuando el líquido es agua. Si se sumerge en líquidos más densos, se hunde menos; por ello, las indicaciones aumentan numéricamente hacia abajo. Según su uso reciben el nombre de pesa‑ácidos, pesa jarabes...
b) Para líquidos menos densos que el agua: La indicación 1, correspondiente a la densidad del agua, la presentan al final de la varilla; al sumergir el aparato en un líquido menos denso, se hunde menos que en ésta, por ello la varilla está graduada en densidades de valor numérico menores que 1 (fig.21.2). Pueden ser: pesa-éteres, pesa alcoholes...

Procedimiento para medir la densidad de un líquido con densímetros
1. Se toma una probeta de 100 o 250 ml y se lava perfectamente. Se enjuaga interiormente con un poco del líquido problema. (El líquido de enjuagar se echa a la pileta con el grifo abierto.)
2. Se elige un densímetro y se introduce con cuidado en la probeta.
3. Si se observa que al soltarlo se va hacia el fondo, se coge, se limpia y se seca y se toma otro densímetro que
mida densidades mayores. Así hasta dar con el adecuado.
4. Ya con el densímetro adecuado, se deja sobre la superficie del líquido dando una rotación con los
dedos de forma que caiga girando.
5. De esta forma, cuando el densímetro se para, se puede medir en su escala sin que se quede adherido
a la pared de la probeta.
6. Tomar la probeta con la mano y subirla hasta conseguir que el nivel del líquido quede a la altura
de los ojos y hacer la lectura de la escala.


La densidad varía con la temperatura, es por lo que una vez se haya medido la densidad, hemos
de medir también la temperatura a la que se ha hecho la medición y luego ver en las tablas
la corrección que debemos hacer.
Estas tablas vienen en la agenda del químico y otros libros de datos de uso frecuente en los laboratorios.
Los areómetros tienen el mismo fundamento que los densímetros, pero en lugar de medir densidades sirven para medirconcentraciones de las disoluciones. Vienen graduados en grados Baumé y pueden ser de dos tipos: a) para disoluciones más densas que el agua (fig. 21.3) y para disoluciones menos densas que el agua (fig. 21.4). 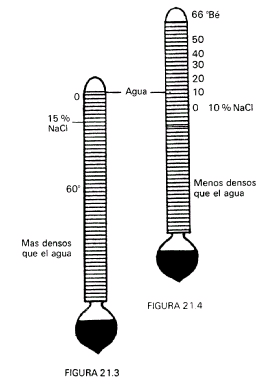
RELACIÓN ENTRE DENSIDAD Y GRADOS BAUMÉ
La relación entre concentración y densidad de una disolución se uti liza todavía en la industria y laboratorios, al dar la concentración de las disoluciones de algunas sustancias en grados Baumé (ºBé), establecidos en 1768. Esta escala equivale a una escala de densidades, tomando como puntos fijos de aquélla el agua pura y una disolución al 10 % de NaCI.
Para líquidos más densos que el agua, la densidad de ésta corresponde a 0º Bé y a la disolución al 10 % de NaCI se le adjudican 10º Bé.
Para líquidos menos densos que el agua se invierten las escalas y el agua pura tiene 10º Bé y a la disolución al 10 % de NaCI le corresponden 0º Bé.
La relación entre ºBé y la densidad depende algo de la temperatura. Para una temperatura ambiente de 15º C se pueden usar las relaciones siguientes:
Líquidos más densos que el agua:
![]()
Líquidos menos densos que el agua:
![]()
Siendo:
n = º Bé (grados BAUMÉ)
d = densidad relativa de la disolución respecto al agua a la misma temperatura
TABLAS DE CONVERSIÓN DE UNIDADES DE MEDIDA
|
|